Atommasse und Mol
Bei der Reaktion von Schwefel mit Eisen reagieren genau 32,1g Schwefel mit 55,8g Eisen vollständig. Bei diesen Mengen bleibt kein Edukt übrig. Es entstehen genau 32,1 + 55,8 = 87,9 g Eisensulfid (FeS). Hat man von einem der Ausgangsstoffe mehr, so bleibt genau dieser Anteil nach der Reaktion übrig. Bei der Reaktion von 64,2g Schwefel und 111,6g Eisen bleibt hingegen kein Ausgangsstoff übrig. Bei diesen Mengen entsteht 87,9 x 2 = 175,8g Schwefelsulfid.
Woher kommt das?
In 32,1g Schwefel sind genau 6 · 1023 Schwefelatome enthalten, in 55,8g Eisen sind genau 6 · 1023 Eisenatome enthalten. Offensichtlich reagieren die Schwefelatome mit den Eisenatomen genau in dem Verhältnis 1:1.
Die Teilchenanzahl 6 · 1023 bezeichnet der Chemiker als 1 mol. Mol ist die Stoffmengeneinheit in der Chemie! 1 mol Schwefel reagieren demnach genau mit 1 mol Eisen vollständig zu 1 mol Schwefelsulfid.
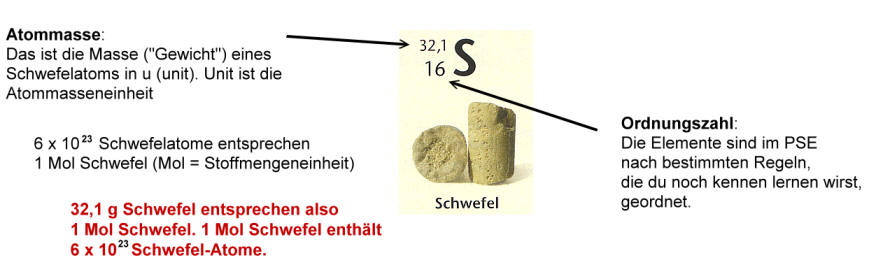
Die Menge in g des Elementes, die genau 1 Mol des Stoffes ausmacht, kannst du im Periodensystem der Elemente (PSE) ablesen: