Basen nach Brønsted
Brønsted bezeichnete Basen als Stoffe, die Protonen aufnehmen können. Wir haben das schon einmal kurz beim Thema Säuren angesprochen, da nach Brönsted Säuren und Basen nicht getrennt voneinander betrachtet werden können.
Ein wesentlicher Unterschied zum Base-Begriff nach Arrhenius ist die Unabhängigkeit vom Wasser. Das folgende Beispiel soll das verdeutlichen:
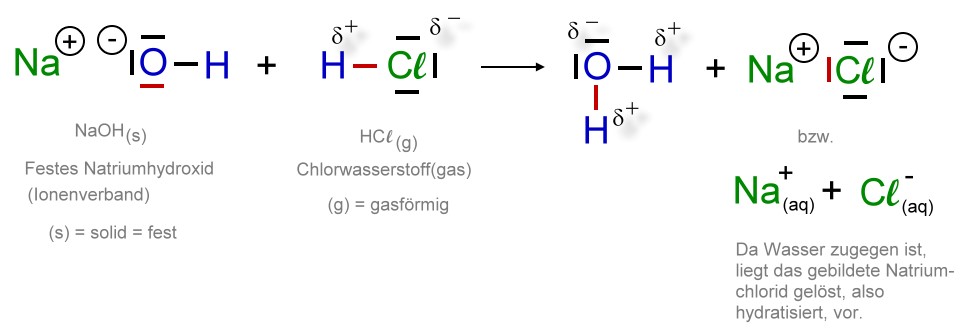 Hier reagieren die Hydroxid-Ionen mit Chlorwasserstoff, ohne, dass für diese Reaktion Wasser nötig ist. Dies wird erst bei der Reaktion gebildet.
Hier reagieren die Hydroxid-Ionen mit Chlorwasserstoff, ohne, dass für diese Reaktion Wasser nötig ist. Dies wird erst bei der Reaktion gebildet.
Das Hydroxid-Ion des Natriumhydroxids ist hier die Brønsted-Base, da es ein Proton aufnimmt. Chlorwasserstoff ist die Brønsted-Säure, da es ein Proton abgibt.
Die Neutralisation von Basen mit Säuren werden wir beim Thema Neutralisation noch ausführlicher besprechen.
Ein anderer wesentlicher Unterschied zwischen der Theorie von Arrhenius und Brønsted ist die Tatsache, dass Brønsted-Basen nicht auf Hydroxid-Ionen begrenzt sind.
Beispiel:
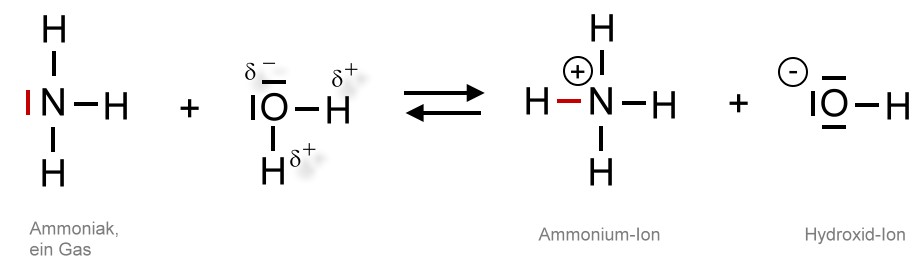
Hier ist Ammoniak eine Brønsted-Base, da Ammoniak-Moleküle Protonen aufnehmen. Wasser ist die Brönsted-Säure, da es ein Proton abgibt. Eine Lösung von Ammonium-Ionen und Hydroxid-Ionen wird auch Ammoniakwasser genannt.
- Alle Basen sind Brønsted-Basen, aber nicht alle Arrhenius-Basen sind Brønsted-Basen.
- Arrhenius-Basen sind nach ihrer Struktur definiert (Metallhydroxide), während Brønsted-Basen durch ihre Funktion Protonen aufzunehmen definiert sind.